Содржина
На корозивни супстанции Тие се оние способни да ги уништат или неповратно да ги оштетат површините со кои доаѓаат во контакт.
Корозивните супстанции се опасни за живи суштества, може да предизвика иритација или изгореници на ткивата на кожата, очите, респираторниот тракт или гастроинтестиналниот тракт што може да доведе до смрт. Овие типови на инциденти се познати како хемиски изгореници.
Овие типови материјали мора да се користат со соодветна изолациска опрема: ракавици, облека, маски за лице. Во местата каде што е депониран или содржан, според меѓународните прописи, наведете со а стандардна икона за корозија.
Општо земено, корозивни супстанции имаат екстремна pH вредност, односно исклучително кисели или базни, иако тие исто така можат да бидат високо оксидирачки супстанции или од друга природа. Во контакт со киселини од органска материја катализираат липидна хидролиза или денатурација на протеини, исто така, резултира со калорично производство чиј заеднички ефект доведува до непоправливо уништување на ткивото. Основите, пак, ја сушат органската материја на екстремен начин.
Примери за корозивни супстанции
- Хлороводородна киселинаНа Со формулата HCl, и исто така познат како муријатична киселина или офортВообичаено е да се извлече од морска сол, или да се произведе дополнително за време на согорување на одредени пластики. Тој е исклучително корозивен и има pH пониска од 1, поради што се користи како растворувач, како индустриски растворувач или како катализатор во производството на други хемиски супстанции.
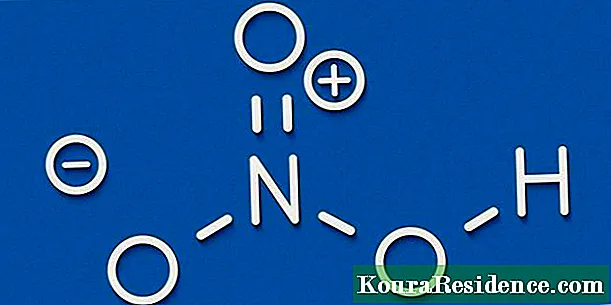
- Азотна киселина. Со формула HNO3, е вискозна течност која најчесто се користи како реагенс во лабораторија, бидејќи е дел од елементите што го сочинуваат Тринитротолуен (ТНТ) или разни ѓубрива како што е амониум нитрат. Исто така, може да се најде растворен во кисел дожд, познат феномен на животната средина последица на загадувањето на водата.
- Сулфурна киселинаНа Неговата формула е Н2ЈУ4 и тоа е еден од најразработените производи во светот, бидејќи често се користи за добивање ѓубрива или за синтеза на киселини, сулфати, па дури и во петрохемиската индустрија. Исто така е корисно во индустријата на челици и во производството на сите видови на батерии.
- Мравја киселинаНа Познат како метаноична киселина и формула CH2ИЛИ2, е наједноставната од органските киселини, често излачувана од инсекти како црвената мравка (Формика руфа) или пчелите како токсичен одбранбен механизам. Исто така, се произведува со коприва, или на кисели дождови поради загадување на атмосферата. Во мали количини може да предизвика мали иритации, но и покрај тоа што е од природно потекло, тоа е силна киселина.
- Концентрирана оцетна киселинаНа Именувана метилкарбоксилна киселина или етаноична киселина и хемиска формула Ц2Х4ИЛИ2, е киселина од оцет, што му дава карактеристичен кисел вкус и мирис. Исто така, е органска киселина, како мравја киселина, но е исклучително слаба, така што нејзините апликации се разновидни и не се ризични. И покрај тоа, во многу високи концентрации може да биде опасно за здравјето.
- Цинк хлоридНа Цинк хлорид (ZnCl2) тоа е цврст повеќе или помалку бели и кристални, многу растворливи во вода, широко користени во текстилната индустрија и како катализатор во лабораторијата. Не е особено токсичен, но во присуство на вода реагира егзотермично (дури и тоа во амбиенталниот воздух) и може да биде особено корозивен, особено за целулоза и свила.
- Алуминиум хлоридНа Со формула AlCl3, Станува збор за а соединение кој има кисели и основни својства истовремено, во зависност од тоа како се разредува. Тој е сиромашен електричен проводник и има ниска точка на топење и точка на вриење, поради што се користи во хемиските процеси како катализатор за реакции, за зачувување на дрвото или за пукање на маслото. Изложеноста на ова соединение е исклучително штетна за телото и може да остави трајни последици за кратко време на изложеност и со брза медицинска помош.
- Бор трифлуоридНа Неговата формула е БФ3 и тоа е безбоен токсичен гас што формира бели облаци во влажен воздух. Често се користи во лабораторија како луисова киселина и при добивање на други соединенија со бор. Тоа е многу силен метален корозивен, кој може да јаде нерѓосувачки челик во присуство на влага.
- Натриум хидроксидНа Каустична сода или каустична сода, со формула NaOH, е многу сушна база која постои како бели кристални и цврсти материи без мирис, чие растворање во вода или киселина генерира голема количина на топлина. Се користи во повеќе или помалку чисти проценти во индустријата за хартија, текстил и детергенти, како и во нафтената индустрија.
- Калиум хидроксидНа Познат како каустичен поташа и со хемиска формула KOH, тоа е многу неорганско соединение за сушење, чија природна корозивност се користи во апликации како сапунификатор на маснотии (во производството на сапун). Неговото растворање во вода е егзотермично, односно генерира топлинска енергија.
- Натриум хидридНа Со формулата NaH, тоа е многу слабо растворлива супстанција со транспарентна боја, класифицирана како а база силен бидејќи е способен за депротонизација на различни лабораториски киселини. Покрај тоа, тој е моќен средство за сушење, бидејќи складира огромни количини на водород, што го прави многу каустичен и се користи како растворувач.
- Диметил сулфатНа Во нормални услови, ова соединение со хемиска формула Ц2Х6ИЛИ4С е безбојна, мрсна течност, со слаб мирис на кромид, наведена како силен алкилатор. Тој е многу токсичен: канцероген, мутаген, корозивен и отровен, така што неговата употреба во лабораториски процеси на метилација нормално се заменува со други побезбедни реагенси. Исто така е еколошки опасно и испарливо, поради што честопати се сметало за веројатно хемиско оружје.
- Фенол (карболна киселина). Хемиска формула В6Х6Или и бројни алтернативни имиња, ова соединение во чиста форма е бела или безбојна кристална цврста материја, која може да се синтетизира од оксидација на бензен. Тоа е во голема побарувачка во индустријата за смоли, како и во производството на најлон, но исто така и како компонента на фунгициди, антисептици и средства за дезинфекција. Лесно е запалив и корозивен.
- Ацетил хлорид. Исто така наречен етаноил хлорид, тоа е халид добиен од етанонска киселина, кој на собна температура и притисок е безбоен. Тоа е соединение што не постои во природата, бидејќи во присуство на вода се распаѓа во етанонска киселина и хлороводородна киселина. Широко се користи како боја, средство за дезинфекција, инсектицид, па дури и како анестетик, и покрај тоа што е корозивен со реакција.
- Натриум хипохлорит. Познат како белило Кога се раствора во вода, ова соединение со хемиска формула NaClO е силен оксидант и високо реактивно со хлор, со што се формираат смртоносно токсични гасови. Широко се користи како белило, прочистувач на вода и средство за дезинфекција, бидејќи во одредени концентрации има способност да раствори органска материја при контакт.
- Бензил хлороформат. Тоа е мрсна течност со непријатен мирис што може да варира од безбојна до жолтеникава и има хемиска формула Ц8Х7ClO2На Опасно за животната средина и водните животни, станува фосфоген кога се загрева и станува многу запалив. Тој е канцероген и многу корозивен.
- Елементарни алкални метали. Секој алкален метал во својата најчиста или елементарна презентација, како што се литиум (Li), калиум (K), рубидиум (Rb), цезиум (Cs) или франциум (Fr), реагира многу брзо со кислород и вода, затоа тие никогаш не се гледано во природата во нивната елементарна состојба. Во двата случаи тие реагираат насилно, генерирајќи многу топлина, поради што можат да бидат иритирачки или каустични и опасни по здравјето.
- Фосфор пентоксид. Познат како фосфор оксид (V) или фосфорен оксид, е бел прав со молекуларна формула Р2ИЛИ5На Да се биде крајно хигроскопски (средство за сушење), има високо корозивни својства и треба да се избегнува каков било контакт со телото. Понатаму, неговото растворање во вода произведува силна киселина која реагира во присуство на метали, генерирајќи отровни и запаливи гасови.
- Калциум оксид. Јавете се вар и со хемиска формула CaO, тоа е супстанција која долго време ја користела човештвото, а која е добиена од варовнички карпи. Има примена во градежништвото и земјоделството, бидејќи не е токсичен или корозивен, но кога се меша со вода реагира егзотермично, така што може да го иритира респираторниот тракт, кожата или да предизвика сериозно оштетување на очите.
- Концентриран амонијак. Нормално, амонијак, безбоен гас со одбивен мирис составен од азот (NH3), се произведува во различни органски процеси кои го елиминираат во животната средина поради неговата токсичност. Всушност, таа е присутна во човечката урина. Сепак, многу од неговите концентрации емитуваат корозивни гасови кои се многу штетни за животната средина, особено во супстанции како што е амонијак анхидрид.
Може да ви служи
- Видови хемиски супстанции
- Примери за хемиски реакции
- Примери за хемиски соединенија
- Примери за киселини и бази